Direction de la recherche clinique et de l’innovation
- Présentation
- Promotions
- Gestion financière
- Cellule de vigilance des essais cliniques
- Unité de Bibliométrie-Pilotage-SIR
- Plateforme méthodologie/biostat
- Actualités
- Aide aux chercheurs
Présentation de la direction de la recherche
La direction de la recherche a pour mission de concevoir, mettre en œuvre et évaluer la politique de recherche de l’établissement (personnels, formation, budgets, développement de la recherche).
Avec la délégation à la recherche clinique (DRCI), elle est chargée de la promotion de la recherche clinique du CHU (procédures administratives et financières).
De plus, en cohérence avec le projet d’établissement et le projet médical, elle formalise avec le président de la commission médicale d’établissement, le vice-président recherche du directoire et le délégué à la recherche clinique, le programme de recherche de l’établissement et des coopérations avec les organismes d’enseignement et de recherche. Elle tient compte des orientations décidées par le comité de la recherche biomédicale et en santé publique.
|
Épidémiologie nationale des surinfections bactériennes lors des pneumopathies acquises sous ventilation mécanique chez les patients infectés par le SARS-COV-2 |
La recherche en santé au CHU de Poitiers, c’est quatre axes thématiques principaux
- Transplantation optimisée – médecine régénératrice (Cellules souches, conservation d’organes, immunité innée) Pr THIERRY
- Technologies en santé . PRISMATICS (Neurostimulation et rachis, chirurgie cardio-thoracique) Pr RIGOARD
. Equipe DACTIM-MIS du Laboratoire de Mathématiques et Applications – CNRS 7348 Pr Rémy GUILLEVIN
. Laboratoire commun CNRS I3M (Imagerie Multimodale Multinoyaux Multiorganes) – Entreprise regroupant les équipes (CNRS) DACTIM-MIS et ICONES ainsi que l’industriel Siemens Pr Rémy GUILLEVIN
- Ophtalmologie (Pathologies dégénératives rétiniennes) Pr LEVEZIEL
- Cancérologie (Tumeurs solides, hémato-cancérologie, plateforme de génétique des cancers) Pr TOUGERON, Pr KARAYAN, Pr LELEU
Appuyée par
Trois unités Inserm labellisées :
 Unité 1082 – Pr HAUET Ischémie reperfusion en transplantation d’organes.Plateforme IBISA de chirurgie expérimentale et transplantation
Unité 1082 – Pr HAUET Ischémie reperfusion en transplantation d’organes.Plateforme IBISA de chirurgie expérimentale et transplantation
- Fédération hospitalo-universitaire (FHU SUPORT) labélisée A+sur la transplantation et la conservation d’organes, en partenariatavec Tours et Limoges.
 Unité 1084 – Pr JABER Laboratoire de neurosciences expérimentales et cliniques (deux équipes : thérapies cellulaires dans les pathologies cérébraleset neurobiologie-neuropharmacologie de l’addiction)
Unité 1084 – Pr JABER Laboratoire de neurosciences expérimentales et cliniques (deux équipes : thérapies cellulaires dans les pathologies cérébraleset neurobiologie-neuropharmacologie de l’addiction)
 Unité 1070 – Pr COUET Pharmacologie des anti-infectieux
Unité 1070 – Pr COUET Pharmacologie des anti-infectieux
Une unité CNRS labellisée :
- Equipe DACTIM-MIS du Laboratoire de Mathématiques et Applications – CNRS 7348 Pr Rémy GUILLEVIN
- Laboratoire commun CNRS I3M (Imagerie Multimodale Multinoyaux Multiorganes) – Entreprise regroupant les équipes (CNRS) DACTIM-MIS et ICONES ainsi que l’industriel Siemens Pr Rémy GUILLEVIN
Un centre d’investigation clinique (CIC1042) labélisé par l’Inserm Infrastructure pour la conduite d’essais cliniques avec matériels et lits d’hospitalisation mis à disposition
Un centre de ressources biologiques (CRB) certifié par l’Afnor Accueil et stockage des échantillons biologiques à des fins de recherche.
Trois équipes d’accueil
- EA 6314 MOVE, Laboratoire mobilité vieillissement et exercice Laurent BOSQUET
 EA 4331 LITEC, Laboratoire inflammation tissus épithéliaux cytokines Pr LECRON
EA 4331 LITEC, Laboratoire inflammation tissus épithéliaux cytokines Pr LECRON
 EA 3808 CIMOTEMA, Cibles moléculaires et thérapeutiques de la maladie d’Alzheimer Pr PAGE
EA 3808 CIMOTEMA, Cibles moléculaires et thérapeutiques de la maladie d’Alzheimer Pr PAGE
Deux équipes émergentes au sein du CIC
- ALIVE, (axe thématique) Lésions pulmonaires aigues Pr ROBERT
- Expologie, Environnement Pr MIGEOT
Les chiffres
En 2015
192 études cliniques ont été nouvellement crées au CHU, dont :
- 22 CHU promoteur
- 2 programmes hospitalier de recherche clinique national (PHRC-N) Pr THILLE, réanimation chirurgicale Dr MCHEK, chirurgie pédiatrique
- 1 programme hospitalier de recherche clinique inter-régional (PHRC-I) Dr COUDROY, réanimation médicale
- Programme de recherche médico-économique (PRME) Pr JAYLE, chirurgie cardiaque
En cours
77 études dont le CHU est promoteur, soit 2 077 inclusions en 2015.
Promotions interne

707 études industrielles et institutionnelles, soit 1 131 inclusions en 2015.
Promotion externe
- 236 études industrielles
- 471 études institutionnelles
- 170 nouveaux dossiers
- 36 contrats uniques
- Dont 6 CHU coordinateur national
Ce qui représente 465 publications dans des revues scientifiques référencées au plan international. Soit un budget de 18 000 000 euros, dont 14 500 000 euros de dotations et 3 500 000 facturation et subventions provenant de sources diverses : ARS, région, Inserm, Inca, CHU, dons et direction générale de l’offre de soins.
Et 300 000 euros de dons de l’association Sport et collection, portant le total à 4 millions d’euros de dons depuis 22 ans.
Un fond de dotation pour appuyer les 3 thématiques :
- Recherche en santé
- Environnement et santé
- Innovation médicale et robotique
Nos partenaires
| Université de Poitiers – Faculté des sciences fondamentales et appliquées |  |
| Grand Poitiers |  |
| Nouvelle Aquitaine |  |
| Union Européenne |  |
| Inra |  |
| Inserm |  |
| CNRS |  |
| FHU SUPORT |  |
| Fonds Aliénor |  |
| Sport et collection |  |
LA PROMOTION INTERNE
L’équipe de la cellule promotion interne a pour mission d’assurer la gestion des études dont le CHU de Poitiers est le promoteur ou l’initiateur.
Les études promues par un autre promoteur institutionnel (autre CHU, CLCC, société savante, etc) étant gérées par la cellule de la promotion externe.
La cellule promotion interne est en charge des études de recherche biomédicale (médicament, dispositif médical, hors produit de santé) mais également des études en soins courants, des études observationnelles et des recherches portant sur les collections biologiques.
Les missions de la cellule promotion interne
- gestion des demandes de promotion en lien avec le délégué régional à la recherche clinique et à l’innovation
- accompagnement des chercheurs dans la constitution des dossiers de réponses aux appels d’offres (PHRC inter régional, PHRC national…)
- établissement des budgets de recherche
- dépôt des autorisations auprès des différentes autorités compétentes (CPP, ANSM, CCTIRS, CNIL, Ministère de la recherche)
- gestion de la logistique des projets et suivi des budgets
- suivi de la qualité de la conduite du projet
- gestion de la vigilance des différents essais
- coordination et supervision des ARC dans la conduite de projet
- rédaction des contrats de recherche pour les financements en collaboration avec la cellule valorisation
Composition de la cellule
Véronique Ferrand-Rigallaud, responsable Demandes de promotion, financements, réponses aux appels d’offres, personnel de recherche Poste : 44 665 veronique.ferrand-rigallaud@chu-poitiers.fr
Fanny Abriat, gestionnaire administrative et logistique Gestion technico réglementaire, suivi des dépenses, logistique Poste : 43 796 fanny.abriat@chu-poitiers.fr
Marie Bonnin, chef de projet Gestion de projet – procédures qualité Poste : 43 317 marie.bonnin@chu-poitiers.fr
Séverine Moussé, biocollections Poste : 43 448 severine.mousse@chu-poitiers.fr
LA PROMOTION EXTERNE
Au sein de la direction de la recherche, la cellule de la promotion externe et de l’innovation a deux fonctions principales :
- la centralisation de la gestion des essais cliniques à promotion industrielle et académique,
- le soutien des équipes médicales qui souhaitent porter et réaliser des projets autour de l’innovation et des thérapeutiques coûteuses.
La composition de la cellule de la promotion externe et de l’innovation :
Sarah Guyon, responsable Téléphone : 05 49 44 39 37 Courriel : sarah.guyon@chu-poitiers.fr
Aude Malézieux, agent administratif Téléphone: 05 49 44 34 04 Courriel : aude.malezieux@chu-poitiers.fr
Morgan Quere Carne, chef de projets
Audrey Moutet, chargée de projets
Les missions de la cellule de la promotion externe et de l’innovation
1 – La promotion externe
Elle a pour mission générale d’assurer le suivi des demandes de mise en place des essais à promotion externe soit les essais industriels et académiques pour lesquels le CHU de Poitiers se positionne en tant que prestataire de service. Son rôle est de réceptionner les demandes de mises en place, de vérifier la complétude du dossier de l’étude auprès du promoteur, d’évaluer les coûts éventuels induits par la recherche en lien avec l’investigateur principal du CHU, dans le but de proposer et de signer in fine une convention hospitalière avec le promoteur. Cette dernière étape est en effet le préalable réglementaire indispensable avant l’autorisation de la conduite de l’étude au sein du CHU.
La cellule de la promotion externe assure le suivi administratif et financier de la mise en oeuvre des essais cliniques à promotion académique ou industrielle de la mise en place de l’étude jusqu’à son terme.
En plus du suivi des recettes affectées à la mise en oeuvre de l’étude, la cellule peut être amenée à gérer les enveloppes « honoraires » des investigateurs qui souhaitent un versement de leurs émoluments à l’hôpital dans le cadre des essais à promotion privée. Dans ce cas, la mise en place de convention tripartite entre le promoteur, l’investigateur et le CHU est préconisée.
La deuxième mission en matière de promotion externe est de recruter et de gérer les personnels de recherche employés par le CHU de Poitiers (exemple : ARC, TEC, Ingénieur, technicien de recherche, IDE de recherche…) sur des fonds externes (aide de l’industrie pharmaceutique, association, INCA, DGOS, CENGEPS…).
Cette coordination s’applique : i) sur le plan de l’évaluation professionnelle et de la formation. Chaque professionnel fait l’objet d’une évaluation professionnelle établie par les médecins investigateurs. Les demandes de formation sont gérées, quant à elles, en lien avec le service de la formation continue, ii) sur le plan financier par le suivi des budgets alloués au personnel et des contrats de travail, iii) sur le plan pratique, en lien avec la direction des ressources humaines pour la signature des contrats.
2 – L’innovation
Elle a pour mission de promouvoir les innovations au sein du CHU de Poitiers en facilitant l’élaboration des protocoles médicaux avec une composante médico-économiques qui sont déposés lors des appels à projets nationaux « Programme de soutien aux techniques innovantes coûteuses – PSTIC». Ce programme de soutien concerne exclusivement les innovations validées dans le cadre d’une étape préalable de recherche clinique et qui présentent un impact potentiel important sur le système de soins. Les STICs sont des projets multicentriques nationaux, financés sur 2 ans, qui permettent la diffusion d’une technique et l’analyse son impact médico-économique par rapport à une prise en charge traditionnelle. Le budget alloué à un STIC est entièrement versé au centre coordonnateur. Ce dernier le répartit sur les différents centres associés au prorata du nombre de patients inclus.
Le STIC hors cancer est coordonné par la direction générale de l’offres de soins (DGOS).
Le STIC cancer est coordonné par l’Institut national du cancer ( INCA) depuis 2005.
Si vous souhaitez coordonner un projet STIC en tant qu’investigateur principal ( PI) ou participer à un projet STIC en tant que co-investigateur, veuillez contacter Sarah Guyon, responsable innovation au 05 49 44 39 37 ou sarah.guyon@chu-poitiers.fr.
L’autre mission de la cellule innovation est de gérer les projets de recherche STIC initiés par le CHU de Poitiers ou par des promoteurs externes. Elle contrôle et suit les budgets des projets STIC, valide les commandes, rédige et suit les conventions financières.
En 2013, le STIC est remplacé par le Programme de recherche médico-économique.
Activité Valorisation au sein de la direction de la recherche et de l’innovation
Née en 2008, l’activité Valorisation est une activité transversale au sein de la direction de la recherche et de l’innovation du CHU de Poitiers. Cette activité permet de protéger les résultats des travaux de recherches ainsi que la propriété intellectuelle issue de l’activité des agents du CHU de Poitiers.
Un partenariat avec le SPVR
Le partenariat et la mutualisation de moyens humains et financiers avec le Service du partenariat et de la valorisation de la recherche (SPVR) de l’université de Poitiers, du CNRS et de l’Ensma, depuis 2008, est un atout pour les chercheurs du CHU.
Ce partenariat facilite la négociation des contrats de partenariats liés à la recherche fondamentale (industriels et/ou institutionnels) et la protection du patrimoine intellectuel (dépôt de demandes de brevets, de créations – droit d’auteur, d’enveloppe Soleau, de marques) détenus en copropriété avec l’université.
L’activité Valorisation
1 – Accords de transfert de matériels biologiques
- Pour tout transfert d’échantillons biologiques humains, un accord de transfert de matériel biologique doit être signé.
Cet accord permet le transfert d’échantillons biologiques humains à un partenaire industriel ou académique. Il a pour objet de régir l’utilisation du matériel, en définissant les responsabilités de chaque partie.
- Ces accords sont également mis en place dans le cadre de l’activité du Centre de Ressources Biologiques, qui garantit la traçabilité et la qualité des échantillons.
Le secteur de la Valorisation est en charge de la rédaction des accords de transfert de matériels biologiques ainsi des contrats de collaboration lorsque des données sont associées.
2 – Propriété intellectuelle
- Protéger les données cliniques et les bases de données, protéger un savoir-faire, protéger un droit d’auteur, une marque, un dessin ou modèle, une invention…
L’activité de valorisation permet de mettre en place une protection au titre du droit d’auteur via le dépôt d’enveloppes SOLEAU auprès de l’Institut national de la propriété intellectuelle (Inpi) à des fins probatoires. Cela recouvre également le dépôt de logiciels auprès de l’Agence de protection des programmes (APP) et la protection de marques via l’enregistrement auprès de l’Inpi.
La propriété industrielle comprend la gestion de dossiers de valorisation en vue d’une étude de brevetabilité, la gestion du portefeuille de brevets en lien avec le Service du Partenariat et de la Valorisation et enfin la gestion des licences d’exploitation de brevets, de logiciels et de savoir-faire.
- Si vous pensez que votre projet peut faire l’objet d’une demande de brevet ou de toute autre protection contactez l’unité de valorisation afin de compléter un dossier de déclaration d’invention.
Comment protéger ?
- Le premier réflexe : l’accord de secret.
Lorsque vous allez discuter de votre projet à des partenaires potentiels, des financeurs privés… Pensez à faire signer un accord de secret.
3 – Activité contractuelle
Au sein de la direction de la recherche, l’activité Valorisation concerne les points d’élaboration, de négociation et de révision des contrats en lien avec les services juridiques de partenaires publics ou privés. Cette activité permet au CHU de protéger son patrimoine intellectuel, en particulier lorsqu’il est promoteur d’essai clinique.
Les questions de propriété intellectuelle et industrielle, dans les contrats de collaboration et de prestations de service, sont traitées en lien avec les porteurs de projets et les partenaires industriels ou académiques.
|
Nous contacter : tel : 05 49 44 33 29 / 05 49 36 63 63 Noëlla Gorry, juriste, chargée d’affaires valorisation – noella.gorry@chu-poitiers.fr |
Unité de gestion budgétaire et financière de la recherche
Contacts
BODIN Muriel, responsable de l’unité (05.49.4)44.330 – murielle.bodin@chu-poitiers.fr
BESNAULT Cecilia, assistante de gestion financière (05.49.4)43.306 – cecilia.besnault@chu-poitiers.fr
Mise en place d’une unité financière de la direction de la recherche et de l’innovation – objectif de la direction générale depuis 2015.
Objectif
Création d’une unité financière en transversalité sur l’ensemble des secteurs de la recherche :
- Donner une définition précise des missions structurées par secteur d’activités et coordonnées entre elles,
- Avoir une comptabilité analytique pour la mesure de la performance de la recherche,
- Avoir une unité transversale pour une vision analytique de l’activité produite et des dotations,
- Avoir un outil de gestion et de pilotage – élément essentiel de la prise de décision stratégique et opérationnelle,
- Avoir un langage commun, de connaitre les coûts des activités réalisées et de comparer les résultats.
Mais aussi évaluer la contribution de chaque secteur pour l’équilibre financier global de la DRC et identifier les leviers d’amélioration au sein des activités.
Missions du responsable de l’unité
Mettre en œuvre et piloter le suivi financier des activités de recherche en coordination transversale sur l’ensemble des secteurs de la recherche.
1. Gestion budgétaire et financière du secteur de la recherche
La diversité des financements associés à la recherche clinique nécessite la mise en œuvre d’une structuration budgétaire pour le suivi des opérations financières des projets de recherche, permettant de justifier le montant des opérations comptabilisées sur le secteur.
La construction budgétaire définie par la DRI a permis de définir des bases d’évaluation de ses activités, tant dans le cadre de la campagne budgétaire MERRI, que dans le cadre des activités subventionnées ou prestations facturées. L’ensemble des charges générées par ses activités sont coordonnées par la DRI permettant le contrôle de la cohérence et de la régularité des opérations financières menées par la recherche.
Le suivi des dotations MIG/MERRI entrant dans le cadre des campagnes budgétaires DGOS devra permettre de gérer les allocations de crédits notifiés sur des indicateurs d’activités de recherche : la gestion de la dotation socle doit prendre en compte la perte d’activité en T2A occasionnée par le temps consacré à la recherche sur les temps hospitaliers dans les pôles et plateaux techniques afin de définir l’impact financier de la mise en œuvre des activités au sein de l’établissement.
Coordonner la gestion financière du secteur « recherche » (en lien la direction des finances), optimiser la gestion des dotations de recherche, veiller à l’application des méthodes comptables : en recettes et en dépenses.
Participer à la certification des comptes de l’établissement grâce à la mise en œuvre d’un dispositif de contrôle au sein de la direction de recherche visant à l’application des recommandations en matière de comptabilisation des opérations financières permettant la présentation d’un EPRD à l’équilibre sur l’exercice comptable.
2. Aider au pilotage stratégique de la recherche
Donner une définition précise des missions structurées par secteur d’activités et coordonnées entre elles pour permettre une vision analytique de l’activité produite, visant à la mesure de la performance en matière de recherche.
Evaluer la contribution de chaque secteur pour l’équilibre financier global de la Direction de la recherche et identifier les leviers d’amélioration pour apporter un aide au pilotage des activités de recherche (connaitre les coûts des activités conduites, mesurer et comparer les résultats) – éléments essentiels de la prise de décisions stratégiques et opérationnelles.
Structurer le tableau des emplois « recherche » dans le cadre du contrôle de la masse salariale « recherche ».
3. Présenter les éléments de suivi financier et comptable des opérations menées par la recherche
Elaborer l’EPRD et suivre son exécution budgétaire, effectuer le suivi des dotations allouées pour la recherche et permettre le développement d’activités.
Coordonner le suivi des projets de recherche dans l’outil informatique EASYDORE : mise en œuvre et développement de l’outil de gestion des projets, budget et personnel.
Participer à la certification des comptes dans le cadre de la mission de suivi comptable.
Suivre les financements des structures de recherche – CIC (Centre d’Investigation Clinique), CRB (Centre de Ressources Biologiques) et de l’ensemble des dotations en MIG pour la recherche.
Effectuer le suivi des dossiers institutionnels, des plateformes et unités de recherche.
Elaborer les rapports financiers : EPRD recherche, compte de résultats recherche, bilans des programmes de recherche.
Fournir les données nécessaires à la constitution du Compte financier du CHU et commentaires.
Participation à des groupes de travail nationaux liés aux financements de la recherche.
Production des données financière pour répondre aux enquêtes DGOS sur les moyens de la recherche.
Missions de l’unité
Au sein de la direction de la recherche, l’unité de vigilance des essais cliniques a pour rôle d’évaluer de façon continue le rapport bénéfice/risque des essais cliniques impliquant la personne humaine promus par le CHU de Poitiers. La vigilance des essais cliniques fait en effet partie des obligations réglementaires du promoteur.
Le champ d’application de la vigilance est large puisqu’il concerne l’analyse et la surveillance des événements indésirables graves survenant dans le cadre d’un essai clinique portant sur un médicament mais également sur un dispositif médical, une technique chirurgicale…
En pratique, l’unité de vigilance des essais cliniques intervient dans un premier temps en amont de la recherche en rédigeant le chapitre sécurité du protocole de recherche (aspects réglementaires, liste d’effets indésirables graves attendus).
Ensuite, l’unité analyse tous les événements indésirables graves survenus lors d’une recherche impliquant la personne humaine, déclarés au promoteur par les investigateurs. Elle évalue la relation entre l’événement et l’essai clinique (imputabilité) ainsi que le caractère attendu ou inattendu de l’événement.
Dans un second temps, une synthèse de la sécurité de l’essai est réalisée au travers du Rapport Annuel de Sécurité (RAS, DSUR).
Si un effet indésirable grave inattendu ou un fait nouveau de sécurité est détecté, une déclaration est réalisée auprès des autorités compétentes (ANSM, EMA via Eudravigilance) et du CPP.
En cas de mise en évidence d’une balance bénéfice/risque défavorable, des mesures urgentes de sécurité seront prises et l’essai clinique pourra être suspendu temporairement ou définitivement.
Télécharger le guide sur la vigilance des essais cliniques.
Composition de l’unité
 Dr Sophie Duranton Praticien hospitalier, pharmacien Tél : (05.49.4)4.30.50 Courriel : sophie.duranton@chu-poitiers.fr
Dr Sophie Duranton Praticien hospitalier, pharmacien Tél : (05.49.4)4.30.50 Courriel : sophie.duranton@chu-poitiers.fr
Marie-Dominique Autexier Attachée de recherche clinique, vigilance des essais cliniques Tél : (05.49.4)4.43.37 Courriel : marie-dominique.autexier@chu-poitiers.fr
Manuela Boué Attachée de recherche clinique, vigilance des essais cliniques Tél : (05.49.4)4.34.69 Courriel : manuela.boue@chu-poitiers.fr
Laura Hamy (relais Girci Soom) Attachée de recherche clinique, vigilance des essais cliniques Tél : (05.49.4)4.46.73 Courriel : laura.hamy@chu-poitiers.fr
La plateforme méthodologie/biostatistique

La plateforme est une unité transversale pour tous les investigateurs et chercheurs du CHU. Elle est prioritairement dédiée à la mise en place et au suivi des essais cliniques ou épidémiologiques dont le CHU de Poitiers est le promoteur.
La plateforme de biométrie occupe une position stratégique au plan institutionnel pour permettre le développement de la recherche clinique et l’évolution des scores bibliométriques. Son champ d’action porte sur les essais cliniques, l’évaluation de dispositifs médicaux, les études diagnostiques et pronostiques, les études observationnelles (cohortes, cas-témoins, registres, etc.).
UF : 9023 Responsable : H. ASTRE, direction de la recherche Coordonnateur Scientifique : D. FRASCA, Pôle USSAR
Méthodologistes-Biostatisticiens
Analyses biostatistiques
Les analyses biostatistiques sont réalisées par les méthodologistes-biostatisticiens conformément au plan d’analyse et à ses amendements.
Les analyses sont prévues et planifiées de façon très précise dès la rédaction du protocole de recherche.
Dans le cadre de questions scientifiques spécifiques, le développement biostatistique de méthodes appropriées fait appel aux collaborations de la plateforme et des équipes de recherche partenaires (Inserm U1246).
Un rapport statistique est établi en suivant les recommandations et procédures opératoires standard (ICH, CDISC). L’interprétation des résultats se fait en collaboration avec l’investigateur.
Les procédures d’analyse statistiques devront suivre les recommandations internationales ICH et du CDISC.
Reférences :
- http://www.ich.org/fileadmin/Public_Web_Site/ICH_Products/Guidelines/Efficacy/E9/Step4/E9_Guideline.pdf
- http://www.cdisc.org/system/files/all/standard/application/pdf/analysis_data_model_v2.1.pdf
Data-Managements

Séverine CLERJAUD
(05.49.4)43.736
severine.clerjaud@chu-poitiers.fr

Florence TARTARIN
(05.49.4)43.267
florence.tartarin@chu-poitiers.fr
Alexandre MANTEAU
(05.49.4)43.359
alexandre.manteau@chu-poitiers.fr
Gestion des données
Une équipe de data-managements est chargée des missions relatives à la collecte et au stockage des données. La planification des opérations de data-management est établie sous la responsabilité du méthodologiste en collaboration avec le data-manager, référents de chaque projet. Les procédures suivent les recommandations du GCDMPC (Good Clinical Data Management Practices Commitee) et de la FDA (notamment 21 CRF part 11).
Références :
- http://www.bvv.sld.cu/docs/libros/__a_119376865712.pdf
- http://www.fda.gov/downloads/ForIndustry/DataStandards/StudyDataStandards/UCM384744.pdf
Missions
- La conception du cahier d’observation et le paramétrage de l’e-CRF avant la mise en place de l’étude
- La conception et mise en place de questionnaires
- Planifier chaque étape clé de la gestion des données pour assurer la cohérence des données (organisation de la saisie, contrôles de cohérence, validité)
- Suivre et gérer l’avancement de la saisie et des queries (messages d’erreurs engendrés par les contrôles de cohérence transmis aux investigateurs) au cours de l’étude
- Organiser la revue des données et le gel de base en fin d’étude
- Réaliser l’archivage sécurisé, en accord avec les exigences réglementaires
Remplir l’imprimé ci-dessous téléchargeable via la docuthèque et l’envoyer à l’adresse suivante : methodologie@chu-poitiers.fr

Les points méthodologiques abordés concernent notamment :
- L’identification des hypothèses de recherche en accord avec le rationnel
- La clarification et hiérarchisation des objectifs
- Le choix des critères de jugement
- Le design des essais
- Le calcul de la taille de l’échantillon nécessaire
- Les procédures de randomisation et d’aveugle
- La rédaction de la partie méthodologie du protocole
- Vérification de la cohérence du protocole final
- Aide à la préparation des protocoles pour le CCTIRS et la CNIL
- Aide pour répondre à des appels à projet
- Suivi méthodologique (amendements, suivi des dysfonctionnements éventuels, préparation du monitorage)
Rédaction médicale et valorisation
Participation à la valorisation scientifique.
Formation
Des actions de formation à destination des étudiants et des personnels hospitalo-universitaires seront organisées. Elles pourront s’intégrer dans la continuité des collaborations avec le GIRCI SOHO.
- Formation des ARC, TEC et investigateurs à l’utilisation des eCRF
- Formation des internes en médecine et pharmacie
- Participation aux enseignements de la faculté de médecine-pharmacie
- Participation aux masters et DU des filières universitaires
- Organisation de séminaires inter-régionaux
Collaborations
- CIC et équipes de recherche CHU – Université de Poitiers
- GIRCI GRAND-OUEST
- GIRCI SOHO
Actualités
- Harold Astre : « L’argent des donateurs permet de démarrer des projets de recherche »
- Ophtalmologie : le CHU s’investit dans la recherche contre la DMLA
- Recherche au CHU : quatre projets financés par le programme hospitalier de recherche clinique
- Recherche : un foisonnement de projets au CHU
- Recherche paramédicale : le CHU ajoute une corde à son arc
- La recherche en ordre de marche
- Recherche sur les perturbateurs endocriniens – Sarah Thévenot : « Une mission de santé publique et un impact concret pour les patients »
- Sport et collection : l’objectif des 4 millions d’euros récoltés en vingt-trois ans sera atteint
- La technopôle Grand Poitiers veut catalyser l’innovation (article paru dans La Nouvelle République du 27 juin 2017)
Aide aux chercheurs
- De l’idée au projet
- Projets à volet médico-économique
- Réglementation dédiée à la recherche
- Procédures institutionnelles dédiées aux chercheurs
- Liens utiles
- Foire aux questions
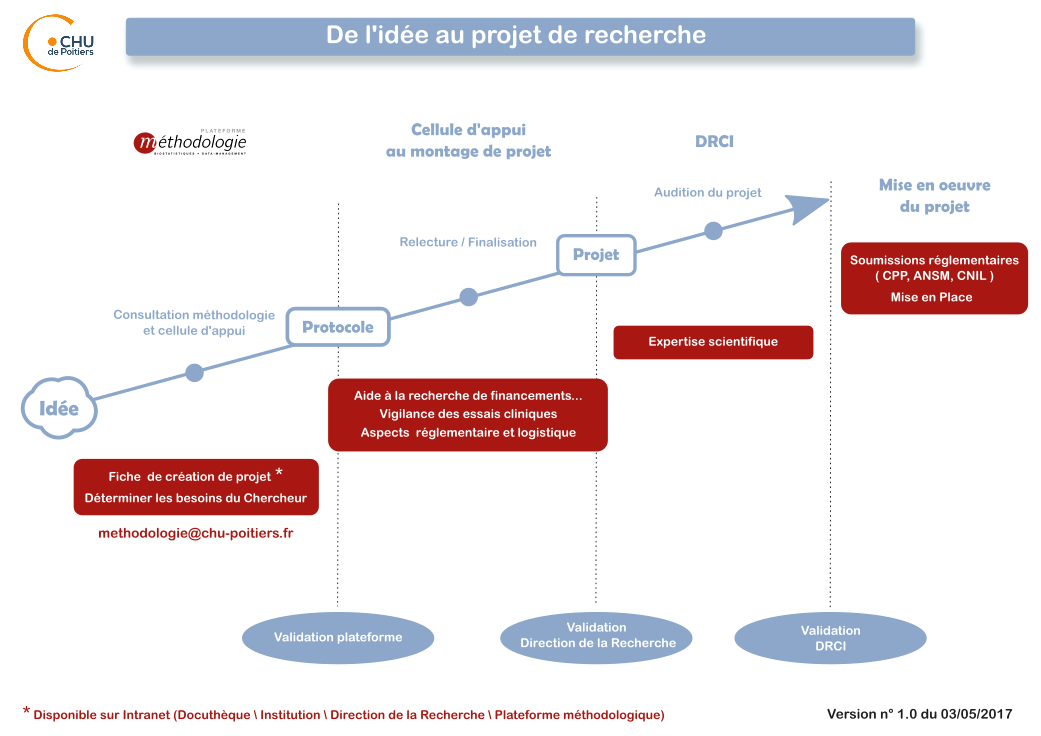
De l’idée au projet
Télécharger la fiche de création de projet.
Projets à volet médico-économique
 Dans le cadre du Girci Soho, le groupe Innovation, évaluation médico-économique et évaluation des technologies de santé, a mis en place une plateforme médico-économique. Son objectif est d’offrir un accès à une expertise méthodologique, par la mise à disposition de ressources en support d’aide au montage de protocoles médico-économique.
Dans le cadre du Girci Soho, le groupe Innovation, évaluation médico-économique et évaluation des technologies de santé, a mis en place une plateforme médico-économique. Son objectif est d’offrir un accès à une expertise méthodologique, par la mise à disposition de ressources en support d’aide au montage de protocoles médico-économique.
Cette plateforme vous permet d’accéder à une aide concernant :
- La méthodologie
- La rédaction de la lettre d’intention
- La rédaction du protocole
- L’analyse médico-économique
- La publication etc.
Pour bénéficier de cette aide, il vous suffit de cliquer sur le lien suivant et de compléter le formulaire associé : https://rc.bespim.fr/surveys/?s=PWTK7AKWJW
Contacter Zoé Pasquier (zoe.pasquier@chu-poitiers.fr) pour plus d’information.
Réglementation dédiée à la recherche
Loi de santé publique n°2004-806 du 9 août 2004 (en vigueur en 2006).
- Loi Jardé n°2012-300 du 5 mars 2012
- Portant sur la personne humaine
- Nouvelle classification des recherches
- Désignation aléatoire d’un CPP
- Précision de certains droits
Règlement Union européenne (RE) n°536/2014 du 16 avril 2014 (application 2018)
- Uniquement pour les médicaments
Loi Touraine n°2016-41 du 26 janvier 2016
- Modernisation du système de santé (articles:155-157-201 et 204)
Ordonnance n°2016-800 du 16 juin 2016
- Adaptation au droit français du futur RE et autres dispositions
- Modification des compétences des CPP régionaux au profit d’un CPP national
- Précision des dispositions transitoires de l’application de la Loi Jardé
Catégories des recherches
- Catégorie 1 (L1121-1) « qui comportent une intervention sur la personne non justifiée par sa prise en charge habituelle » RBM médicament, hors produits de santé et dispositif médical
- Catégorie 2 (L1121-1) « qui ne portent pas sur des médicaments et ne comportent que des risques et des contraintes minimes » (cf. l’arrêté du 2 décembre 2016) Ex soin courant mais aussi RBM hors produits de santé, dispositif médical
- Catégorie 3 (L1121-1) « Dans lesquelles tous les actes sont pratiqués et les produits utilisés de manière habituelle, sans procédures supplémentaires ou inhabituelle de diagnostic, de traitement ou de surveillance». Observationnelle, thèse prospective, …….
Les recherches sur données (rétrospectives, sur dossier médical) ne rentrent pas le champ d’application de la loi Jardé : recherche impliquant la personne humaine.
Procédures institutionnelles dédiées aux chercheurs
| Numéro | Titre de la procédure | Version, date | ||
| DRC | MEP | 001 | Mettre en place un centre investigateur | V3, Fév 2016 |
| DRC | MON | 001 | Effectuer une visite de monitoring sur un centre investigateur | V3, Mars 2016 |
| DRC | MON | 002 | Gérer les déviations d’un centre investigateur | V1, Déc 2013 |
| DRC | MON | 003 | Effectuer le monitoring des consentements des patients | V1, Fév 2014 |
| DRC | DOC | 001 | Gérer la documentation sur un centre investigateur | V3, Mars 2016 |
| DRC | DOC | 002 | Gérer la documentation d’une étude promue par le CHU | V1, Déc 2013 |
| DRC | DOC | 004 | Archiver les documents d’une étude | V1, Nov 2013 |
| DRC | DOC | 005 | Numéroter, nommer et archiver les versions des documents d’une étude | V1, Juil 2014 |
| DRC | VIGI | 001 | Gérer les EvI survenus dans le cadre des protocoles de recherche biomédicale | V3, Janv 2014 |
| DRC | VIGI | 002 | Assurer la continuité de l’évaluation des données de sécurité | V1, Août 2016 |
| DRC | VIGI | 003 | Gérer la levée de l’aveugle | V2, Juil 2014 |
| DRC | VIGI | 004 | Gestion d’un EvIG reçu par le Département Vigilance | V1, Mai 2016 |
| DRC | VIGI | 005 | Gérer une query à partir du logiciel Safety Easy | V1, Mai 2016 |
| DRC | VIGI | 006 | Saisie d’un EvIG sur le logiciel Safety Easy | V1, Mai 2016 |
| DRC | VIGI | 007 | Gestion des alertes mails reçus par le Département Vigilance | V1, juin 2016 |
| INS | REC | 12 | Comité indépendant de surveillance | V2, Oct 2013 |
| INS | REC | 13 | Convention de codage MedDra | V1, Mai 2012 |
| INS | REC | 15 | Document de référence | V1, Mai 2012 |
| INS | REC | 16 | Rédaction de la partie sécurisée d’un protocole | V1, Mai 2012 |
| DRC | GPE | 001 | Gérer le circuit et effectuer le monitoring des PE | V2, Jan 2015 |
| DRC | CLO | 001 | Effectuer une visite de clôture | V2, Fév 2014 |
| DRC | GRC | 004 | Evaluer le niveau de risque et le grade de monitoring d’une étude | V1, Mar 2015 |
| DRC | RGL | 001 | Procéder aux instructions administratives avant la MEP d’un essai clinique | V1, Juin 2014 |
| DRC | FDR | 001 | Intégrer les nouveaux ARCs et TECs | V1, Mars 2016 |
Liens utiles
- Girci Soom
- ANSM
- Inserm
- Ministère des Affaires sociales et de la Santé
- LEEM
- CCTIRS
- Aide financière aux chercheurs (Nouvelle Aquitaine)
- Fondation Allianz
- CNRS
Foire aux questions
Quels éléments doivent apparaître dans la lettre d’information ?
Selon l’article L.1122-1 du code de la santé publique, doivent maintenant être précisés dans la lettre d’information, certains éléments relatifs à la recherche :
L’objectif de la recherche, la méthodologie, la durée, les bénéfices attendus, les contraintes, les risques prévisibles, y compris en cas d’arrêt prématuré de la recherche, les éventuelles alternatives médicales. Les modalités de prise en charge médicales prévues en fin de recherche , si une telle prise en charge est nécessaire, en cas d’arrêt prématuré de la recherche, et en cas d’exclusion de la recherche
L’avis du CPP, et l’autorisation de l’ANSM.
Le droit d’avoir communication, au cours ou à l’issue de la recherche, des informations concernant sa santé et qui sont détenues par l’investigateur .
Le cas échéant, l’interdiction de participer simultanément à une autre recherche ou la période d’exclusion prévue par le protocole et son inscription dans le fichier national des personnes soit ne présentant aucune affection et se prêtant volontairement à la recherche, soit malades lorsque l’objet de la recherche est sans rapport avec leur état pathologique. Le droit pour la personne dont le consentement est sollicité, de refuser de participer à la recherche ou de retirer son consentement à tout moment sans avoir à se justifier et sans conséquence sur la prise en charge.
Les modalités permettant à la personne d’être, à l’issue de la recherche, informée des résultats globaux de cette recherche.
Devront aussi être précisées, bien que non mentionné dans l’article L.1122-1 du code de la santé publique, les modalités de protection du secret professionnel et du respect de la vie privée selon les modalités prévues par la loi n° 78-17 relative à l’informatique, aux fichiers et aux libertés, dans sa version consolidée au 7 août 2004 (ou modifiée par la loi n° 2004-801 du 6 août 2004) et notamment :
Les personnes qui seront habilitées à consulter le dossier médical,
L’utilisation prévue des données personnelles,
Le droit d’accès et de rectification aux informations personnelles concernant la personne et détenues dans le cadre de la recherche, selon les modalités des articles 39 et 40 de la loi informatique et libertés précitée, avec mention de la personne responsable à qui s’adresser pour exercer ce droit.
Attention, il existe toutefois des cas particuliers :
Cas des personnes mineures non émancipées ou protégées, et des majeurs protégés ou hors d’état de donner leur consentement (article L.1122-2, I du code de la santé publique) : Ils reçoivent une information adaptée à leur capacité de compréhension, tant de la part de l’investigateur que des personnes chargées de les assister, de les représenter ou d’autoriser la recherche, eux-mêmes informés par l’investigateur. Ils sont consultés dans la mesure où leur état le permet. Leur adhésion personnelle en vue de leur participation à la recherche biomédicale est recherchée. En toute hypothèse, il ne peut être passé outre à leur refus ou à la révocation de leur acceptation .
Quelles sont les mesures introduites dans la réglementation suite à « l’accident de Rennes » de janvier 2016 ?
Il s’agit de mesures spécifiques ayant pour objet de renforcer la protection des personnes et notamment des volontaires sains se prêtant à des essais correspondant à une première administration ou utilisation chez l’homme d’un médicament ou d’un autre produit de santé.
Concernant les autorisations de lieux de recherches (articles L. 1121-13 et R. 1121-13 du CSP), délivrées par les Agences régionales de santé (ARS), celles-ci sont valables pour :
- une durée de 3 ans pour les lieux où se dérouleraient des essais de première administration à l’homme d’un médicament,
- une durée de 7 ans dans les autres cas.
Concernant les notifications relatives à la vigilance des essais :
- Quelles sont les dispositions nouvelles en matière de notification de cas ?
- A) Délai de déclaration des effets indésirables : Pour les recherches portant sur les médicaments, les dispositifs médicaux et les recherches ne portant pas sur un produit de santé, le promoteur notifie les effets indésirables graves inattendus qui entraînent la mort ou la mise en danger de la vie sans délai.
- B) Des dispositions particulières ont été introduites concernant les essais portant sur le médicament menés chez des volontaires sains (quelle que soit la phase de l’essai) (article R. 1123-54 du CSP).
Ainsi, pour ces essais, les promoteurs déclarent :
- les événements indésirables graves, ainsi que les effets indésirables graves attendus et inattendus (à savoir tout événement et effet indésirable qui entraîne la mort, met en danger la vie de la personne qui se prête à la recherche, nécessite une hospitalisation ou la prolongation de l’hospitalisation, provoque une incapacité ou un handicap importants ou durables, ou bien se traduit par une anomalie ou une malformation congénitale, et quelle que soit la dose administrée) ;
- à l’ANSM ;
- sans délai.
S’agissant d’une disposition issue de la réglementation française, celle-ci s’applique aux cas survenus sur le territoire français. Toutefois, le promoteur peut également notifier à l’ANSM les cas survenus dans l’essai à l’étranger.
Est- ce que l’ajout de nouveaux investigateurs constitue une modification substantielle ?
L’ajout de nouveaux investigateurs est considéré comme une modification substantielle en vertu de :
1- art. L1123-7 : « Le comité rend son avis sur les conditions de validité de la recherche, notamment au regard de : la qualification du ou des investigateurs
2 – art.R 1123-35 : « Les modifications substantielles mentionnées à l’art L. 1123-9 sont celles qui ont un impact significatif sur tout aspect de la Recherche……y compris…..sur les conditions de validité de la Recherche…..sur les modalités de la conduite de celle-ci. »
3 – Seul le CPP donne un avis sur la qualification des investigateurs art. : R 1123-35 « l’Autorité Compétente et le CPP se prononcent sur les modifications substantielles apportées par rapport aux éléments du dossier qui leur a été initialement soumis ».
N’hésitez pas à envoyer vos questions à l’adresse suivante : marilyne.dellion@chu-poitiers.fr